标的公司:CytomX Therapeutics,Inc.(NASDAQ:CTMX)
CytomX Therapeutics,Inc.(CTMX)宣布II期CX-2029治疗晚期鳞状非小细胞肺癌(sqNSCLC)或头颈鳞状细胞癌(HNSCC)患者的初步结果,CX-2029是由CytomX和AbbVie共同开发的CD71定向条件性激活抗体药物结合物(ADC)。

截至2021年10月29日数据截止,23例SDSNCLC患者和29例HNSCC患者在3mg/kg(安全人群)中接受了至少一种CX-2029剂量,其中16例SnSnCLC患者和25名HNSCC患者至少有一次基线评估(疗效评估人群),包括每个方案,5名患者(2例sqNSCLC和3例HNSCC)入选B部分(肿瘤活检组)。中位随访时间为3.8个月(range,0.2-20.1)。在16例sqNSCLC疗效可评估患者中,客观缓解率(ORR)为18.8%,包括两个已确认的部分缓解率(PRs)和一个在数据截止后7天确认的PR。疾病控制率(DCR)为87.5%,其中包括完全缓解、PR或病情稳定的患者。在25例可评估疗效的HNSCC患者中,有1例确认PR(ORR4.0%)和56.0%的DCR,包括1例未确认PR。下表为汇总表。
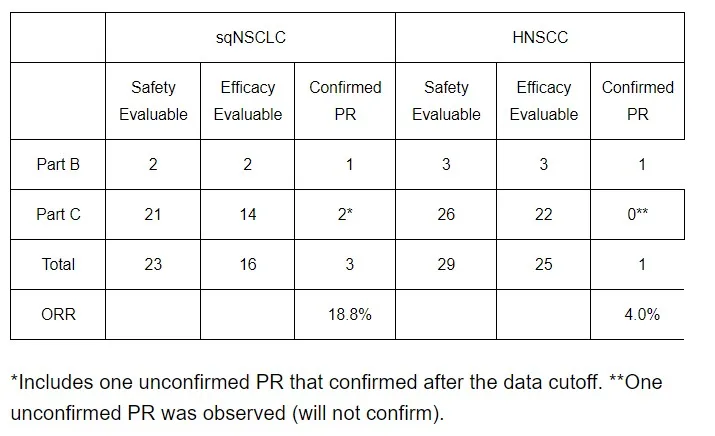
在B部分(N=5)或扩展组(N=47)中,对至少服用一剂3mg/kg CX-2029(N=52)的所有sqNSCLC和HNSCLC患者进行安全性分析。对于sqNSCLC和HNSCLC,先前转移治疗的中位数分别为2(范围1-5)和3(范围1-9)。所有sqNSCLC患者均接受过铂和检查点抑制治疗;在HNSCC中,除一名患者外,所有患者均接受过铂治疗,除两名患者外,所有患者均接受过检查点抑制治疗。
安全状况与I期观察结果一致,未发现新的安全信号。在10%或以上的患者(所有级别,3级)中,最常见的治疗相关不良事件(TRAE)为贫血(78.8%,67.3%)、输液相关反应(69.2%,3.8%)、疲劳(19.2%,1.9%)和恶心(13.5%,0.0%)以及中性粒细胞计数下降(13.6%,9.6%(加上一个4级事件1.9%)。停药最常见的原因是疾病进展(44.2%),3名患者(5.8%)因治疗相关不良事件(贫血;2级,1级3)而停药。导致剂量中断或减少的TRAE分别为40.4%和34.6%。截至数据截止,13名患者,其中8名为sqNSCLC,5名为HNSCC,仍在接受治疗。
CX-2029
CX-2029由CytomX和AbbVie共同开发,是一种条件激活抗体-药物结合物(ADC),由CD71导向的人源化单克隆抗体组成,通过可切割连接物与微管抑制剂单甲基auristatinE(MMAE)结合,药抗比(DAR)为2。CX-2029的一个关键特征是其掩蔽肽,覆盖并阻断抗体的细胞结合区。掩蔽肽通过蛋白酶可切割连接物与抗体相连,设计用于在富含蛋白酶的肿瘤微环境中去除,使随后未掩蔽的ADC能够与其靶结合并在肿瘤细胞内传递毒性有效载荷。目标是使CX-2029在循环中保持惰性,目的是限制健康组织中的结合,直到被肿瘤相关蛋白酶激活。CX-2029在II期扩展研究(NCT03543813)中作为单一疗法评估,将患者纳入四个组;鳞状非小细胞肺癌、鳞状头颈癌、食管和胃食管交界癌(腺癌和鳞状组织学)以及弥漫性大B细胞淋巴瘤。
CytomX Therapeutics
CytomX是一家专注于肿瘤治疗的生物制药公司,致力于以不同方式消灭癌症。CytomX开创了一种新型的条件激活生物制剂,由Probody®技术平台提供动力,其目标是超越当前癌症治疗的局限性,成功利用曾经被认为无法达到的治疗靶点。CytomX强大且分化的生产线包括全资拥有的praluzatamab-ravtansine(CX-2009),一种针对CD166的研究性条件性激活抗体药物结合物(ADC),以及CX-2029,一种针对CD71的研究性条件性激活ADC,与AbbVie共同开发。这两个项目目前正在II期研究中进行评估,针对各种晚期、难以治疗的癌症类型,包括praluzatamab-ravtansine治疗的乳腺癌,以及CX-2029治疗的鳞状非小细胞肺癌和头颈鳞状细胞癌
未经允许不得转载:美股开户者 » CytomX:盘前-22%,II期ADC药物CX-2029扩展研究,治疗HNSCC和sqNSCLC
 美股开户者
美股开户者