标的公司:Galera Therapeutics,Inc.(NASDAQ:GRTX)
Galera Therapeutics,Inc.(GRTX)宣布,其avasopasem针对局部晚期头颈癌(HNC)患者放疗诱导的严重口腔粘膜炎(SOM)的3期ROMAN试验的校正结果,在降低SOM发病率的主要终点上有统计学意义。
该公司先前宣布,在SOM中进行的阿瓦索帕西姆3期ROMAN试验在主要终点上没有达到统计学意义。经进一步分析,合同研究组织(CRO)在统计程序中发现了一个错误。纠正此错误后,主要和次要终点的p值得到改善。

校正后的p值如下所示:
- 与安慰剂组(64%)相比,avasopasem治疗组(54%)的SOM发病率相对降低16%(p=0.0451*)(先前报告为p=0.113)(主要终点)
- 治疗组(8天)与安慰剂组(18天)的SOM发生天数相对减少56%(p=0.0022*)(以前报告为p=0.011)(次要终点)
- 与安慰剂组(33%)相比,治疗组SOM严重程度(4级OM发生率)相对降低27%(p=0.052)(之前报告为p=0.167)(次要终点)
该公司还宣布了其在欧洲进行的avasopasem单臂2a期EUSOM试验的topline结果,该试验用于接受标准治疗RT+顺铂的HNC患者的RT诱导SOM。这项试验在欧洲六个国家的12个中心进行,共招募了38名患者,其中33人完成了全面治疗。普遍耐受良好。在EUSOM中,SOM的发病率为54.5%,SOM的中位数天数为9天,与ROMAN试验一致,该试验的发病率为54%,中位数持续时间为8天。
在美国,每年约有42000名HNC患者接受标准治疗RT,并有SOM,即影响饮食能力的口腔疼痛。在市场研究中,放射肿瘤学家和患者都认为SOM是HNC治疗中最沉重的RT毒性。目前,还没有FDA批准的药物可以降低实体瘤中SOM的发生率或持续时间。
美国食品和药物管理局(FDA)已授予avasopasem突破性治疗指定(BTD),以减少RT诱导的SOM。
Galera Therapeutics,Inc.
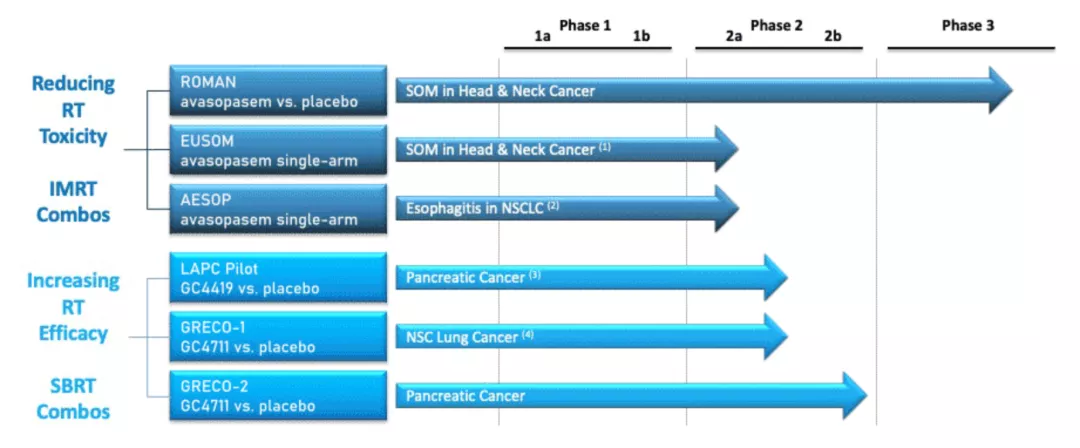
Galera Therapeutics,Inc.是一家临床阶段的生物制药公司,专注于开发和商业化一系列新颖、专有的候选治疗药物,有可能改变癌症的放射治疗。Galera的选择性歧化酶模拟产品候选avasopasem manganese(GC4419,也称为avasopasem)正在评估放疗诱导的毒性。该公司的第二个候选产品rucosopasem manganese(GC4711,也称为rucosopasem)正处于临床阶段,旨在增强立体定向全身放疗对非小细胞肺癌和局部晚期胰腺癌患者的抗癌疗效。
未经允许不得转载:海外华人美股开户 » Galera:+95%,口腔粘膜炎3期avasopasem统计校正结果达到主要终点
 海外华人美股开户
海外华人美股开户