标的公司:AIM ImmunoTech Inc. (NASDAQ:AIM)
AIM ImmunoTech Inc. (AIM)是一家免疫制药公司,专注于研究和开发治疗多种癌症、免疫疾病和病毒性疾病的疗法,包括由SARS-CoV-2病毒引起的COVID-19,今天宣布公布来自晚期复发性卵巢癌腹膜内化学免疫治疗的1/2期研究的阳性数据。题为“Phase I trial combining chemokine-targeting with loco-regional chemo-immunotherapy for recurrent, platinum-sensitive ovarian cancer shows induction of CXCR3 ligands and markers of type 1 immunity”的文章发表在美国癌症研究协会出版的临床癌症研究上。
匹兹堡大学医学院正在进行的1/2期研究旨在评估强化局部区域序贯腹膜内(IP)顺铂(IPC)与静脉(iv)紫杉醇随后腹膜输注趋化因子调节(CKM)方案,该方案由腹膜内林他莫德和干扰素-α(IFNα)的混合物组成,用于晚期卵巢癌(III-IV)患者的初级新辅助治疗。AIM ImmunoTech为1/2期研究提供了rintatolimod(Ampligen®,一种dsRNA,作为TLR3激动剂)。
12名患者参加了试验的1期部分,并接受了IP顺铂、IP Ampligen® 和口服塞来昔布(COX-2阻滞剂)治疗。第2、3和4组的患者也分别接受了2、6和1800万单位的IP IFNα。该研究的主要目标是评估安全性、确定第2阶段推荐剂量和表征免疫TME的变化。腹膜常驻细胞和IP灌洗液分别通过NanoString和Meso Scale Discovery (MSD) 多重分析进行分析。
在参加该1期试验的12名患者中,可评估安全性、毒性和其他终点的有9名(75%)。由于铂类超敏反应或输液港并发症,3名不可评估的患者未完成至少3个周期的治疗。总体而言,除了最高剂量的IFNα外,该方案的耐受性良好。所有级别最常见的毒性是贫血(58%)、低镁血症(50%)、低钠血症(41.7%)、关节痛(41.7%)和疲劳(41.7%)。有1例4级低镁血症(8.3%)。在两名接受18MU IFNα的患者(队列4)中出现了3级或更高级别的腹痛的剂量限制性毒性。
2期推荐的IFNα剂量为每3周600万单位。中位PFS为8.4(3-16.4)个月。中位总生存期为30(8-66)个月。公司相信这些生存结果数据提供了一个令人鼓舞的早期信号。总体反应率为55.6%,疾病控制率(DCR)为77.8%,与预期的铂敏感反应一致。在响应者中,响应的中位持续时间为11.7(6-16.4)个月。
研究结果要点:
- 确定局部顺铂、Ampligen和IFNα联合口服塞来昔布的安全性和2期推荐剂量;
- 通过腹腔内灌洗取样获得了化学免疫疗法组合触发腹膜常驻细胞的转录组变化;
- 腹腔内灌洗液的蛋白质含量捕获治疗诱导的IFN诱导的免疫效应分子增加;
- 间隔减瘤时的肿瘤免疫谱显示与IP灌洗部分重叠,并指出编码穿孔素和颗粒酶B的基因上调。
通过腹腔内灌洗采样显示干扰素刺激基因的局部上调,包括CTL吸引趋化因子(CXCL-9、-10、-11)、MHCI/II、穿孔素和颗粒酶。这些变化在趋化因子调节后两天出现并在一周内消退。
基于这些令人鼓舞的结果,公司计划支持一项后续2期试验,该试验将明确定义肿瘤负载αDC1疫苗与顺铂/趋化因子调节组合方案的免疫学和临床疗效。
关于AIM ImmunoTech Inc.
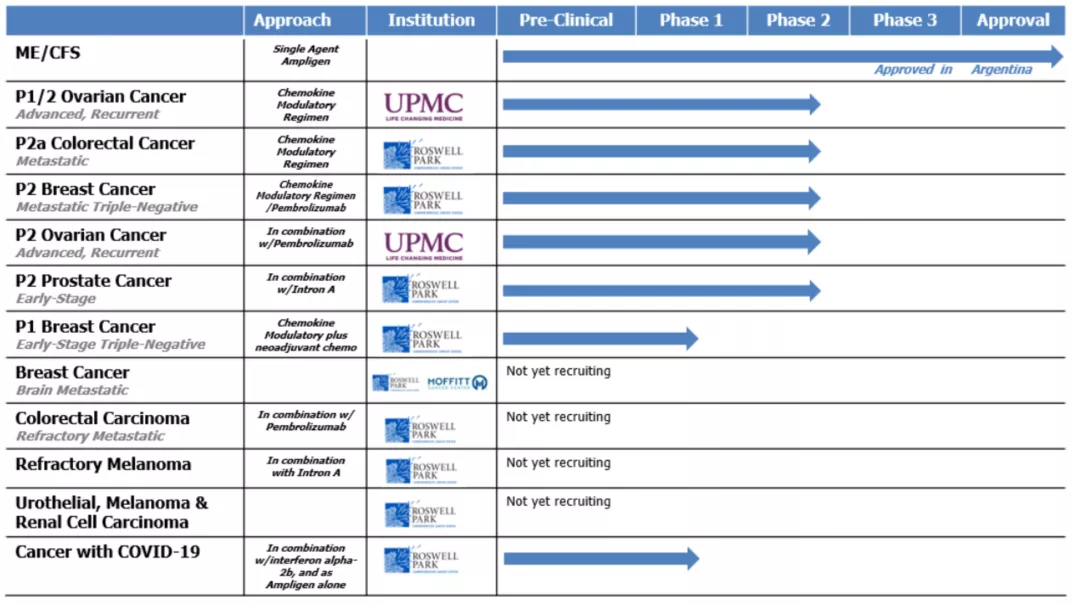
AIM ImmunoTech Inc.是一家免疫制药公司,专注于研究和开发治疗多种癌症、免疫疾病和病毒性疾病的疗法,包括由SARS-CoV-2病毒引起的疾病COVID-19。
未经允许不得转载:美股开户者 » AIM ImmunoTech:公布卵巢癌1/2期试验的阳性数据
 美股开户者
美股开户者